Современная наука стремится сделать геномные технологии не только более эффективными, но и максимально безопасными для медицины и биотехнологий. Команда исследователей из МГУ, Сколтеха и ИТЭБ РАН совершила качественный скачок в этой области — они научились управлять точностью и селективностью геномного редактирования с помощью температурных «выключателей», встроенных прямо в редактор ДНК. Этот подход основан на инновационной работе с молекулярным механизмом BspD6I и оказывает важное влияние на развитие технологий, подобных CRISPR/Cas9.
Перспективы точного редактирования: мотив и задачи исследований
Геномная инженерия продолжает оставаться одной из самых активно развивающихся областей современной биотехнологии. Несмотря на популярность CRISPR/Cas9, существует значительный спрос на методы, которые позволят проводить тонкую точечную коррекцию ДНК, минимизировать риск ненужных мутаций и максимально повысить гибкость манипуляций с геномом. Одно из ключевых ограничений классических технологий заключается в их широкой «зоне охвата» — часто для исправления одной ошибки приходится вмешиваться во фрагмент ДНК длиной в десятки нуклеотидов. Это далеко не всегда приемлемо, особенно для терапии болезней или создания высокоточных биосенсоров.
Инновационные ферменты: BspD6I как альтернатива традиционным системам
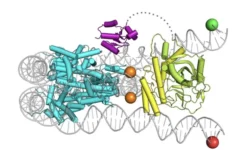
В стремлении к созданию более деликатных и управляемых инструментов ученые активно исследуют природные эндонуклеазы. Важная особенность таких ферментов, как BspD6I, состоит в их умении точечно устранять отдельные нуклеотиды в одной из цепей молекулы ДНК, оставляя неповрежденной вторую цепь. Благодаря этому снижается вероятность случайных мутаций, что особенно ценно для медицинских применений. Эти ферменты были впервые подробно изучены в Институте теоретической и экспериментальной биофизики РАН и с тех пор стали предметом глубоких прикладных и фундаментальных исследований.
Температурное управление: принцип работы и преимущества технологии
Российские ученые увидели необычную закономерность: если добавить к BspD6I специальные короткие нити ДНК — так называемые олигонуклеотиды, — функционирование фермента можно существенно затормозить. Эти молекулы как бы «замораживают» активность геномного редактора при комнатной температуре. Но стоит среде нагреться, начинается обратимый процесс — блокирующие олигонуклеотиды распадаются, освобождая BspD6I для работы по прямому назначению. Поразительно, что температуру срабатывания можно настраивать — она зависит от длины олигонуклеотида, то есть систему легко адаптировать для конкретных условий или жизнеобеспечения разных организмов.
Такой «термостат» позволяет запускать геномное редактирование с высокой временной и температурной избирательностью. Генетический инструмент становится «умным»: он функционирует лишь тогда, когда это действительно необходимо, затрагивая только нужные участки ДНК без риска глобального вмешательства во всю молекулу.
Экспериментальные результаты и гибкость новой технологии
Испытания системы прошли на фрагментах ДНК бактериофага T7 — классического объекта молекулярной биологии. Было выявлено, что при 25°C эндонуклеаза BspD6I практически полностью заблокирована и не проявляет активности. Но стоит повысить температуру до 45°C, как запускается полноценное редактирование: фермент точно разрезает целевые последовательности в ДНК, устраняя только дефектные участки.
Яркое преимущество состоит в том, что изменения температуры напрямую регулируют всю работу редактора, а число «букв» в олигонуклеотиде задает необходимый порог для срабатывания. Это открывает огромные возможности для гибкой настройки экспериментальных процедур, моделирования биологических процессов и даже создания многоуровневых молекулярных сигналов для живых клеток.
Возможности для медицины и биотехнологий: новый этап развития
Создание «температурного переключателя» в системе редактирования ДНК — это не просто технологическое новшество. Такой подход потенциально позволяет программировать реакции клеток на самые разные стимулы, что необходимо для разработки умных биосенсоров, генной терапии и диагностических систем нового поколения. Уже сейчас становится понятно: подобные решения будут играть ключевую роль в выращивании трансгенных организмов, коррекции заболеваний, моделировании злокачественных клеток и синтезе «живых схем», управляемых сигналами среды.
Кроме того, способность пунктуального включения и выключения работы ферментов гарантирует биобезопасность экспериментов и предотвращает нежелательные мутационные процессы, расширяя сферу использования таких редакторов в клинической практике и фундаментальной науке.
Будущее за интеллектуальными редакторами: оптимизм и вдохновение
Применение температурно-чувствительных олигонуклеотидов в комбинации с точечными эндонуклеазами на примере BspD6I — это важный шаг к созданию интеллектуальных генетических инструментов, которые можно сравнить с биологическими чипами. Гибкость и надежность таких систем дают ученым из МГУ, Сколтеха и ИТЭБ РАН уникальные инструменты для проектирования биологических процессов с точностью и безопасностью, недостижимых прежде.
Остается лишь с радостью ждать дальнейших разработок и внедрения подобных технологий в практику медицины и биотехнологий, где каждое новое решение — это открытие возможностей для спасения и улучшения жизни миллионов.
Изображение: Фотобанк Freepik
Источник: scientificrussia.ru